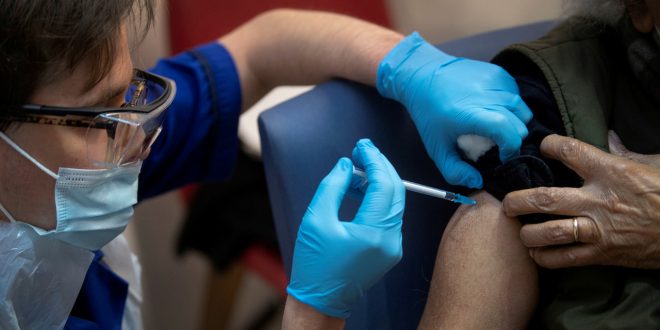
Регистрацию вакцины предложили провести по ускоренной процедуре в чрезвычайных обстоятельствах
Профильный комитет Управления по вопросам качества продовольствия и медикаментов (FDA) при Министерстве здравоохранения и социальных служб США порекомендовал руководству управления одобрить вакцину от коронавируса Pfizer/BioNTech. Об этом сообщает ТАСС.
Эксперты FDA призвали одобрить регистрацию вакцины по ускоренной процедуре в чрезвычайных обстоятельствах.
В ходе финального голосования сотрудники комитета утвердительно ответили на вопрос о том, превышает ли польза от использования вакцины сопутствующие риски. Руководство управления рассмотрит рекомендации комитета и примет решение по заявке «настолько быстро, насколько это возможно».
Отмечается, что управление лишь однажды выдавало разрешение по упрощенной процедуре — на вакцину от сибирской язвы в 2005 году.
Ранее сообщалось, что только 47 процентов американцев готовы привиться от коронавируса, когда в стране будут сертифицированы вакцины от заболевания.
К настоящему моменту в мире зарегистрированы несколько вакцин против COVID-19. В России одобрены две вакцины: «Спутник V» и «ЭпиВакКорона». 5 декабря в Москве стартовала вакцинация от коронавируса препаратом «Спутник V». В США зарегистрирована вакцина от COVID-19 производства Pfizer/BioNTech, на очереди еще одна вакцина Moderna.
 Русские новости Будь в курсе страны
Русские новости Будь в курсе страны